Cách viết phương trình hóa học lớp 10
Bài tập phương trình chất hóa học lớp 10 về halogen là một trong những phần kiến thức rất quan trọng đặc biệt trong công tác Hóa học tập lớp 10. Sau đây, kiến Guru trình làng tới các em học viên phần tóm tắt định hướng và phương thức giải, ví dụ như minh họa kèm bài tập vận dụng để triển khai bài tập phương trình chất hóa học lớp 10 về halogen.
Bạn vẫn đọc: bài bác tập cân đối phương trình chất hóa học lớp 10 tất cả đáp án

– nỗ lực rõ đặc điểm vật lý đặc trưng và đặc thù hóa học của các halogen với hợp chất của bọn chúng .+ Halogen là phần đa phi kim nổi bật. Tính oxi hoá giảm dần đi trường đoản cú F đến I. Các halogen đứng trước vẫn đẩy halogen thua cuộc nó thoát khỏi dung dịch muối halogen .+ F trong tổng thể các hợp hóa học chỉ tất cả số oxi hoá 1 vì gồm độ âm điện to nhất. Những nguyên tố halogen còn lại còn tồn tại các số oxi hoá + 1, + 3, + 5, + 7 .+ Tính khử của HX tăng ngày một nhiều từ HF cho HCl mang lại HBr đến HI.+ Tính axit của dung dịch HX tăng nhiều từ HF cho HCl mang lại HBr cho HI.
Bạn đang xem: Cách viết phương trình hóa học lớp 10
+ Tính axit của HXO4 sút dần từ HClO4 đến HBrO4 mang lại HIO4 .
Ví dụ 1.
f ) CrO3 + HC l → CrCl3 + Cl2 + H2O
Hướng dẫn:
a ) 2C l2 + 2C a ( OH ) 2 → CaCl2 + Ca ( OCl ) 2 + 2H2 Ob ) KClO3 + 6HC l → KCl + 3C l2 + 3H2 Oc ) 6KOH + 3C l2 → 5KC l + KClO3 + 3H2 Od ) Cl2 + SO2 + 2H2 O → 2HC l + H2SO4e ) Fe3O4 + 8HC l → FeCl2 + 2F eCl3 + 4H2 O
f ) 2C rO3 + 12HC l → 2C rCl3 + 3C l2 + 6H2 O
Ví dụ 2: dứt các phương trình chất hóa học theo sơ trang bị sau (ghi rõ đk phản ứng).
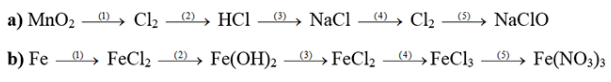
Hướng dẫn:
a )
1. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O2. Cl2 + SO2 + 2H2O → 2HCl + H2SO43. 2Na + 2HCl → 2NaCl + H24. 2NaCl + 2H2O → H2 ↑ + 2NaOH + Cl2
5. Cl2 + 2NaOH → NaCl + NaClO + H2O
b )
1. Fe + HCl → FeCl2 + H22. FeCl2 + NaOH → Fe(OH)2 + NaCl3. Fe(OH)2 + 2HCl → FeCl2 + 2H2O4. 2FeCl2 + Cl2 → 2FeCl3
5. FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl
Câu 1. Viết phương trình hóa học của bội nghịch ứng tiến hành các biến hóa dưới đây, ghi tên các chất và điều kiện của làm phản ứng.
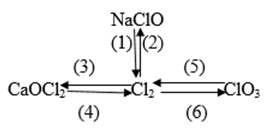
Đáp án:
( 1 ) Cl2 + 2N aOH → NaCl + NaClO + H2O( 2 ) NaClO + 2HC l → NaCl + Cl2 + H2O( 3 ) Cl2 + Ca ( OH ) 2 rắn → CaOCl2 + H2O( 4 ) CaOCl2 + 2HC l → CaCl2 + Cl2 + H2O( 5 ) 3C l2 + 6KOH → 5KC l + KClO3 + 3H2 O
( 6 ) KClO3 + 6HC l → 3C l2 + KCl + 3H2 O
Câu 2. Ta tiến hành sục khí Cl2 vào hỗn hợp KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào?
A. KCl, KClO3, Cl2 .B. KCl, KClO3, KOH, H2O .C. KCl, KClO, KOH, H2O .
D. KCl, KClO3 .
Đáp án: B
3C l2 + 6 KOH → 5KC l + KClO3 + 3H2 O
Câu 3. Ta tiến hành sục khí Cl2 vào dung dịch KOH loãng, nguội, dư. Dung dịch thu được có những chất thuộc hàng nào?
KCl, KClO3 .
Đáp án: C
Cl2 + 2 KOH → KCl + KClO + 3H2 O
Câu 4. Cho các chất sau: Zn (2), KOH (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), K2SO4 (6). Axit HCl chức năng được với những chất:
A. ( 1 ), ( 2 ), ( 4 ), ( 5 ) .
B. (3), (4), (5), (6).
C. ( 1 ), ( 2 ), ( 3 ), ( 4 ) .D. ( 1 ), ( 2 ), ( 3 ), ( 5 ) .
Đáp án: A
HCl + KOH → KCl + H2OZn + 2HC l → ZnCl2 + H2Al ( OH ) 3 + 3HC l → AlCl3 + 3H2 O
2KM nO4 + 16HC l → 5C l2 + 2KC l + 2M nCl2 + 8 H2O
Câu 5. Cho các chất sau : Zn (1), CuO (2), Ag (3), Al(OH)3 (4), KMnO4 (5), FeS (6), MgCO3 (7), AgNO3 (8), MnO2 (9), PbS (10). Axit HCl không công dụng được với những chất :
A. ( 1 ), ( 2 ) .B. ( 3 ), ( 4 ) .C. ( 5 ), ( 10 ) .
D. ( 3 ), ( 10 ) .
Đáp án: D
Ag thua cuộc H2 trong dãy chuyển động hóa học tập → không chức năng được cùng với axit HCl với H2SO4 loãng .PbS ko phản ứng vì chưng là muối không tan trong axit .
FeS cũng là muối ko tan nhưng lại tan được trong axit .
*Một số xem xét về muối bột sunfua
– muối sunfua tung trong nước : K2S, Na2S, ( NH4 ) 2S, BaS, …– muối bột sunfua ko tan vào nước dẫu vậy tan trong HCl, H2SO4 loãng : ZnS, FeS, MnS, …– muối sunfua không tan vào nước cùng không tan trong HCl, H2SO4 loãng : PbS, CuS, Ag2S, CdS, SnS, HgS …
– muối hạt sunfua không sống sót trong nước : MgS, Al2S3, …
Câu 6. Cho những phản ứng:
( 1 ) O3 + hỗn hợp KI →( 2 ) F2 + H2O – to →( 3 ) MnO2 + HCl đặc – khổng lồ →( 4 ) Cl2 + hỗn hợp H2S →Những phản bội ứng nào tạo thành đơn hóa học ?A. ( 1 ), ( 2 ), ( 3 ) .B. ( 1 ), ( 3 ), ( 4 ) .C. ( 2 ), ( 3 ), ( 4 ) .
D. ( 1 ), ( 2 ), ( 4 ) .
Đáp án: A
( 1 ) O3 + 2KI + H2O → I2 + O2 + 2KOH( 2 ) 2F2 + 2H2 O – khổng lồ → O2 + 4HF( 3 ) MnO2 + 4HC l sệt – to → Cl2 + MnCl2 + 2H2 O
( 4 ) 4C l2 + H2S + 4H2 O → H2SO4 + 8HC l
Câu 7. Cho sơ đồ gửi hóa:
Fe3O4 + dung dịch HI ( dư ) → X + Y + H2OBiết X với Y là loại sản phẩm ở đầu cuối của các bước chuyển hóa. Các chất X cùng Y là :A. Fe và I2 .B. FeI3 và FeI2 .C. FeI2 cùng I2 .
D. FeI3 cùng I2 .
Xem thêm: Chí Tài " Huyền Thoại Linh Xe Ôm Tài Chó Điên Remix, Linh Xe Ôm Và Tài Chó Điên Remix
Đáp án: C
Fe3O4 + 8HI → 3F eI2 + I2 + 4H2 O
Câu 8. Cho sơ đồ:
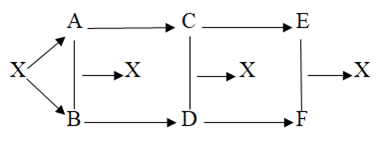
Viết những phản ứng xảy ra theo sơ vật trên với X là NaCl .
Đáp án:
2N aCl ( đp ) → 2N a + Cl22N a + Cl2 → 2N aCl2N a + 2H2 O → 2N aOH + H2Cl2 + H2 → 2HC lNaOH + HCl → NaCl + H2O2N aOH + H2SO4 → Na2SO4 + 2H2 O2HC l + tía ( OH ) 2 → BaCl2 + 2H2 O
Na2SO4 + BaCl2 → BaSO4 ↓ + 2N aCl
Kiến Guru hi vọng thông qua bài viết này, những em học sinh sẽ nắm rõ kiến thức về tính chất đặc trưng của các halogen cùng hợp chất. Sát bên đó, những em cũng đã biết đến và ghi nhớ những dạng, nhiều bài tập phương trình hóa học lớp 10 về halogen.
Chúc những em học tốt !
Điều hướng bài viết
Source: https://camnangbep.com Category: học hành
Bài viết tiên tiến nhất
Tả Cây Mít Lớp 4 ❤ ️ ️ 15 bài xích Văn Tả Về Cây Mít, quả Mít tuyệt ✅ các Bài Văn Đặc nhan sắc Đạt Điểm Cao Giúp các Em học viên Tham Khảo Để Ôn Tập tốt . Những…
Chuỗi phản ứng hóa học lớp 10 Chương Halogen được lingocard.vn soạn là chuỗi các phản ứng hóa học 10, giúp các bạn học sinh rèn luyện với những phương trình từ đó ghi nhớ các tính chất, bí quyết hóa học một giải pháp nhanh nhất. Mời các bạn tham khảo.
Hoàn thành sơ đồ dùng phản ứng
Bài 1: Viết các phương trình bội phản ứng xảy ra cho những sơ thiết bị sau:
a. HCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2 → AgCl
b. KMnO4 → Cl2 → HCl → FeCl3 → AgCl→ Cl2→ Br2 → I2
c. KMnO4 → Cl2 → HCl → FeCl2 → AgCl → Ag
d. HCl → Cl2→ FeCl3 → Fe(OH)3 → Fe2(SO4)3
e. HCl → Cl2 → NaCl → HCl → CuCl2 → AgCl → Ag
f. MnO2 → Cl2 → KClO3 → KCl → HCl → Cl2 → Clorua vôi
Đáp án hướng dẫn giải bài xích tập
a. HCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2 → AgCl
4HCl + MnO2
Cl2 + MnCl2 + 2H2O
3Cl2 + 2Fe

2FeCl3
3NaOH + FeCl3 → 3NaCl + Fe(OH)3
H2SO4 + NaCl → HCl + NaHSO4
CuO + 2HCl → 2H2O + CuCl2
2AgNO3 + CuCl2 → 2AgCl + Cu(NO3)2
b. KMnO4 → Cl2 → HCl → FeCl3 → AgCl→ Cl2→ Br2 → I2
(1)16HCl + 2KMnO4 → 5Cl2 + 8H2O + 2KCl
(2) H2 + Cl2
2HCl
(3) Fe2O3 + 6HCl → 3H2O + 2FeCl3
(4) 3AgNO3 + FeCl3 → 3AgCl + Fe(NO3)3
(5) 2AgCl → 2Ag + Cl2
(6) Cl2 + 2KBr → Br2 + 2KCl
(7) Br2 + 2HI → I2 + 2HBr
c. KMnO4 → Cl2 → HCl → FeCl2 → AgCl → Ag
2KMnO4 +16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Cl2 + H2
2HCl
2HCl + sắt → FeCl2 + Cl2
FeCl2 + 3AgNO3→ Fe(NO3)3 +2AgCl + Ag
2AgCl
2Ag + Cl2
d. HCl → Cl2→ FeCl3 → Fe(OH)3 → Fe2(SO4)3
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2Fe + 3Cl2
Đang xem: Phương trình hóa học lớp 10 hk2
b. KMnO4 → Cl2 → HCl → CuCl2 → BaCl2 → BaSO4.
c. NaCl → HCl → Cl2 → FeCl3 → NaCl → NaOH → NaCl → Cl2 → CaCl2 → AgCl →Ag.
d. NaCl → HCl → KCl → Cl2 → NaCl → H2 → HCl → Cl2 → CuCl2 → Cu(OH)2 → CuSO4 K2SO4 → KNO3.
Bài 3: Viết những phương trình màn biểu diễn dãy biến hóa sau (ghi rõ điều kiện).
b. Cl2 → FeCl3 → NaCl → Cl2 → Br2 → HBrO → NaBrO.
c. H2 → HCl → Cl2 → FeCl2 → Fe(NO3)2 → Fe(OH)2 → FeSO4 → FeCl2 → AgNO3.
Bài 4: Hãy biểu diễn sơ đồ đổi khác các hóa học sau bằng phương trình hoá học:
a. NaCl + H2SO4 → Khí (A) + (B)
b. (A) + MnO2 → Khí (C) + rắn (D) + (E)
c. (C) + NaBr → (F) + (G)
d. (F) + NaI → (H) + (I)
e. (G) + AgNO3→ (J) + (K)
f. (A) + NaOH → (G) + (E)
Đáp án lý giải giải
A là HCl; B là Na2SO4; C là Cl2; D là MnCl2; E là H2O; F là Br2; G là NaCl; H là NaBr; I là I2; J là NaNO3; K là AgClPhương trình hóa họca. 2NaCl + H2SO4
Na2SO4 + 2HCl
b. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
c. Cl2 + 2NaBr → Br2 + 2NaCl
d. 2NaI + Br2 → 2NaBr + I2
e. NaCl + AgNO3 →NaNO3 + AgCl
f. HCl + NaOH → NaCl + H2O
Bài 5: khẳng định A, B, C, D và xong các phương trình bội nghịch ứng sau:
a. MnO2 + (A) → MnCl2 + (B)↑ + (C)
b. (B) + H2 → (A)
c. (A) + (D) → FeCl2 + H2
d. (B) + (D) → FeCl3
e. (B) + (C) → (A) + HClO
Đáp án lý giải giải
a) MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
b) Cl2 + H2
2HCl
c) 2HCl + sắt
FeCl2 + H2
d) 3Cl2 + 2Fe
2FeCl3
e) Cl2 + H2O → HCl + HClO
A là HCl; B là Cl2; C là H2O; D là Fe
Bài 6: xác định A, B, C, D, E, F, G:
HCl + MnO2 → (A) + (B) rắn + (C) lỏng.
(A) + sắt → FeCl3.
(A) + (C) → (D) + (E)
(D) + Ca(OH)2 → (G) + (C).
(F) + (E) → (C)
(F) + (A) → (D).
………………………………………………..
Trên đây lingocard.vn đã trình làng tới bạn đọc tài liệu: Chuỗi bội nghịch ứng hóa học lớp 10 Chương Halogen.Để có công dụng cao hơn trong học tập tập, lingocard.vn xin ra mắt tới chúng ta học sinh tài liệu chất hóa học lớp 10, Thi thpt quốc gia môn Văn, Thi thpt tổ quốc môn lịch sử, Thi thpt quốc gia môn Địa lý, Thi thpt tổ quốc môn Toán, đề thi học tập kì 1 lớp 11, đề thi học kì 2 lớp 11 mà lại lingocard.vn tổng hợp và đăng tải.
Ngoài ra, lingocard.vn đã ra đời group chia sẻ tài liệu học tập trung học phổ thông miễn chi phí trên Facebook, mời độc giả tham gia team Tài liệu tiếp thu kiến thức lớp 10 để sở hữu thể cập nhật thêm nhiều tài liệu new nhất.









